Sửa đổi Luật Dược: Khắc phục những bát cập, hạn chế về đăng ký lưu hành thuốc, nguyên liệu làm thuốc
12/04/2024 | 14:04 PM
Tại phiên họp thẩm tra sơ bộ về Dự án Luật sửa đổi, bổ sung một số điều của Luật Dược, đại diện cơ quan soạn thảo cho biết, việc sửa đổi Luật căn cứ vào nhiều cơ sở thực tiễn, đặc biệt là việc sửa đổi này sẽ khắc phục những bất cập, hạn chế liên quan về đăng ký lưu hành thuốc, nguyên liệu làm thuốc, đảm bảo phù hợp chủ trương cải cách hành chính
Trình bày Tờ trình tại phiên họp thẩm tra sơ bộ, đại diện cơ quan soạn thảo cho biết, Luật Dược được Quốc hội khóa XIII thông qua ngày 06/4/2016, thay thế cho Luật Dược năm 2005, đánh dấu một bước phát triển quan trọng trong việc hoàn thiện hệ thống pháp luật về dược tại Việt Nam, cơ bản phù hợp với sự phát triển của ngành dược trong xu thế hội nhập quốc tế. Theo đó, Luật Dược 2016 ra đời đã điều chỉnh toàn diện các vấn đề liên quan đến chính sách của Nhà nước về dược và phát triển công nghiệp dược; hành nghề dược; kinh doanh dược; đăng ký, lưu hành, thu hồi thuốc và nguyên liệu làm thuốc; dược liệu và thuốc cổ truyền; đơn thuốc và sử dụng thuốc; thông tin thuốc, cảnh giác dược và quảng cáo thuốc; dược lâm sàng; quản lý thuốc trong cơ sở khám bệnh, chữa bệnh; thử thuốc trên lâm sàng và thử tương đương sinh học của thuốc; quản lý chất lượng thuốc, nguyên liệu làm thuốc và quản lý giá thuốc.
Luật Dược đã góp phần tạo lập môi trường đầu tư kinh doanh bình đẳng, thông thoáng, tạo thuận lợi tối đa cho doanh nghiệp, người dân cơ bản đã được bảo đảm cung ứng đủ thuốc có chất lượng với giá cả hợp lý, ngành công nghiệp dược trong nước đạt mức độ phát triển ở trình độ cao, đạt cấp độ 3,5 theo thang phân loại của Tổ chức Y tế Thế giới (WHO), có giá trị thị trường trong tốp 3 ASEAN, góp phần bảo đảm cung ứng đầy đủ, kịp thời thuốc có chất lượng, an toàn, hiệu quả và giá hợp lý; huy động tối đa các nguồn lực trong và ngoài nước cho đầu tư phát triển kinh tế - xã hội.
Thứ trưởng Bộ Y tế Đỗ Xuân Tuyên trình bày Tờ trình
Sau hơn 07 năm triển khai thi hành Luật, ngành dược đã đạt được nhiều thành tựu quan trọng, các quy định của pháp luật về dược đã tạo cơ sở pháp lý sự phát triển theo hướng công khai, minh bạch, nhất là trong bối cảnh hội nhập kinh tế toàn cầu. Thông qua các cơ chế, chính sách, văn bản pháp luật về dược đã được ban hành, ngành dược Việt Nam đã phát triển mạnh mẽ góp phần vào công tác bảo vệ, chăm sóc sức khỏe cho người dân.
Tuy nhiên, trước những yêu cầu và đòi hỏi cấp bách từ thực tiễn, hệ thống pháp luật về dược đã bộc lộ một số hạn chế, bất cập, cụ thể: Một số quy định liên quan về đăng ký lưu hành thuốc, nguyên liệu làm thuốc đã bộc lộ bất cập và chưa phù hợp chủ trương cải cách hành chính
Về hồ sơ, trình tự, thủ tục gia hạn hiệu lực giấy đăng ký lưu hành (Giấy ĐKLH) đối với thuốc, nguyên liệu làm thuốc: Khoản 1 Điều 56 Luật Dược quy định tất cả các thuốc sau khi hết hạn hiệu lực Giấy ĐKLH thì đều phải nộp lại hồ sơ gia hạn và các hồ sơ này đều phải trải qua quá trình thẩm định, xét duyệt của Hội đồng tư vấn cấp Giấy đăng ký lưu hành. Quy định này của Luật Dược đã góp phần giúp cho việc quản lý thuốc có chất lượng, an toàn và hiệu quả.
Tuy nhiên, chỉ phù hợp với các thuốc trong quá trình lưu hành có vấn đề về chất lượng hoặc an toàn cần phải đánh giá lại trước khi gia hạn hiệu lực Giấy ĐKLH. Đối với thuốc trong thời gian lưu hành trên thị trường không nhận được những phản ánh liên quan đến chất lượng, an toàn cho người sử dụng hoặc không có khuyến cáo của Tổ chức Y tế Thế giới thì việc thẩm định, xét duyệt lại hồ sơ gia hạn của Hội đồng tư vấn là không cần thiết vì nếu phải chờ thẩm định, phê duyệt để tiếp tục được gia hạn hiệu lực Giấy ĐKLH có thể làm gián đoạn việc lưu hành thuốc, nguyên liệu làm thuốc trên thị trường dẫn đến đứt gãy nguồn cung tạm thời đồng thời gây quá tải cho Hội đồng tư vấn, gây ách tắc, chậm cấp phép và tồn đọng hồ sơ.
Thường trực Ủy ban Xã hội thẩm tra sơ bộ dự án Luật Dược (sửa đổi)
Khoản 3 Điều 56 Luật Dược quy định hồ sơ gia hạn hiệu lực Giấy ĐKLH phải nộp 06 loại tài liệu, chủ yếu là các tài liệu về hành chính, Luật Dược quy định nộp một số tài liệu này trong bối cảnh việc cấp phép lưu hành lần đầu trước đây chưa áp dụng hệ thống cấp giấy phép lưu hành thuốc trực tuyến (online). Hiện nay, Bộ Y tế đã triển khai hệ thống cấp phép trực tuyến và trong thời gian tới sẽ liên thông cơ sở dữ liệu được quốc gia thì hoàn toàn tra cứu lại được các tài liệu này nên không cần thiết phải yêu cầu nộp lại. Việc phải nộp nhiều tài liệu trong hồ sơ đã dẫn đến lãng phí thời gian, nguồn lực cho doanh nghiệp khi chuẩn bị hồ sơ cũng như tạo áp lực cho cơ quan quản lý trong việc phải thẩm định, xét duyệt hồ sơ.
Về trình tự, thủ tục cho phép thay đổi, bổ sung Giấy ĐKLH thuốc, nguyên liệu làm thuốc, khoản 1 Điều 56 Luật Dược quy định việc thay đổi, bổ sung Giấy ĐKLH thuốc, nguyên liệu làm thuốc phải thông qua thẩm định hồ sơ, tư vấn của Hội đồng tư vấn cấp Giấy ĐKLH thuốc, nguyên liệu làm thuốc. Quy định này của Luật Dược cũng giúp cho việc quản lý thuốc có chất lượng, an toàn và hiệu quả. Tuy nhiên, trong tình hình hiện nay, quy định về trình tự, thủ tục này là không cần thiết đối với các trường hợp chỉ thay đổi về hành chính đơn giản (thay đổi địa chỉ thư tín, thay đổi cách viết tên, địa chỉ cơ sở sản xuất, đăng ký thuốc, bổ sung mã QR, barcode...) không liên quan đến chuyên môn kỹ thuật, an toàn, hiệu quả của thuốc, gây lãng phí thời gian cho doanh nghiệp đồng thời tạo áp lực về thời gian giải quyết thủ tục hành chính cho cơ quan quản lý nhà nước.
Bên cạnh đó, quy định này cũng chưa hội nhập với các nước trên thế giới, trong khu vực (giao cho cơ sở tự công bố, chịu trách nhiệm hoặc chỉ cần thông bảo cho cơ quan quản lý nhà nước để hậu kiểm...). Vì vậy, cần thiết phải phân hóa cụ thể các trường hợp thay đổi, bổ sung để quy định trình tự, thủ tục tương ứng nhằm tạo thuận lợi cho doanh nghiệp và phù hợp thông lệ quốc tế.
Các đại biểu nghiên cứu tài liệu tại phiên họp
Về thử thuốc trên lâm sàng đối với thuốc khi đăng ký lưu hành đối với thuốc dược liệu có sự kết hợp mới của dược liệu đã từng sử dụng làm thuốc tại Việt Nam, điểm b khoản 1 Điều 89 quy định thuốc thuốc dược liệu có sự kết hợp mới của dược liệu đã từng sử dụng làm thuốc tại Việt Nam và có chỉ định đối với các bệnh thuộc danh mục do Bộ trưởng Bộ Y tế ban hành phải thử lâm sàng đầy đủ các giai đoạn khi đăng ký lưu hành.
Quy định này có 02 cách hiểu khác nhau trong việc xác định trách nhiệm của Bộ trưởng Bộ Y tế về ban hành danh mục thuốc cổ truyền có sự kết hợp mới của dược liệu đã từng sử dụng làm thuốc tại Việt Nam hay Danh mục các bệnh chỉ định, đã dẫn đến khó khăn trong quá trình hướng dẫn triển khai thi hành Luật Dược, vì: Khoản 7 Điều 2 Luật Dược quy định thuốc dược liệu là thuốc có thành phần từ dược liệu và có tác dụng dựa trên bằng chứng khoa học. Theo đó, các thuốc dược liệu mới hoặc thuốc có sự kết hợp mới của dược liệu đã được lưu hành, sử dụng muốn đăng ký chỉ định mới thì phải có đầy đủ dữ liệu lâm sàng đáp ứng các quy định chung về thử nghiệm lâm sàng của WHO, EMA, US-FDA...
Theo quy định của quốc tế, về nguyên tắc, các yêu cầu khi đăng ký lưu hành đối với thuốc dược liệu là tương tự như thuốc hỏa dược. Hiện nay, chưa có cơ quan quản lý nào ban hành danh mục chỉ định đối với thuốc dược liệu để yêu cầu phải thử lâm sàng đầy đủ các giai đoạn. Vì vậy, quy định tại điểm b khoản 1 Điều 89 không phù hợp với quy định của Việt Nam và của Quốc tế, cần thiết phải bãi bỏ.
.jpg) Phó Chủ nhiệm Ủy ban Xã hội Nguyễn Hoàng Mai đề nghị tiếp tục đánh giá tác động đối với những chính sách mới của Dự án Luật
Phó Chủ nhiệm Ủy ban Xã hội Nguyễn Hoàng Mai đề nghị tiếp tục đánh giá tác động đối với những chính sách mới của Dự án Luật
Tại phiên họp thẩm tra sơ bộ, cơ quan thẩm tra tán thành sự cần thiết sửa đổi, bổ sung một số điều của Luật Dược căn cứ vào cơ sở chính trị, pháp lý và cơ sở thực tiễn như Tờ trình của cơ quan soạn thảo. Tuy nhiên cơ quan thẩm tra đề nghị tiếp tục đánh giá tác động đối với những chính sách mới của Dự án Luật; đảm bảo việc đánh giá tác động này phản ánh chi tiết, cụ thể sự ảnh hưởng của chính sách đối với từng vấn đề có liên quan./.
Nguồn: Quochoi.vn
Tin liên quan
- Bộ trưởng Đào Hồng Lan: Y tế Việt Nam và khát vọng vươn mình trong kỷ nguyên mới
- Bộ trưởng Bộ Y tế Đào Hồng Lan thăm, chúc Tết tại Bệnh viện Phụ sản Trung ương
- Thủ tướng Chính phủ Phạm Minh Chính chúc Tết, kiểm tra công tác ứng trực tại Bệnh viện Bạch Mai và Bệnh viện Hữu nghị Việt Đức
- Bộ trưởng Bộ Y tế Đào Hồng Lan thăm, chúc Tết một số đơn vị y tế
- Thứ trưởng Bộ Y tế Lê Đức Luận thăm, chúc Tết, kiểm tra công tác khám chữa bệnh tại 2 Bệnh viện và Công ty vắc xin và Sinh phẩm Số 1
- Thứ trưởng Bộ Y tế Lê Đức Luận thăm, làm việc và chúc Tết tại tỉnh Lào Cai
- Thứ trưởng Thường trực Bộ Y tế Vũ Mạnh Hà: Chuyến xe yêu thương nối dài hy vọng cho người bệnh ung thư về quê đón Tết
 Xuất bản thông tin
Xuất bản thông tin
Tết Bính Ngọ, chàng trai 21 tuổi hiến tạng sau chết não, 4 cuộc đời được hồi sinh
Thứ Hai, ngày 23/02/2026 10:35Từ nghĩa cử hiến tạng của người bệnh chết não, sự sống được trao gửi lại cho 4 bệnh nhân đang ở ranh giới mong manh sinh- tử. Bốn cuộc đời bước qua cánh cửa tuyệt vọng để trở về với sự sống......
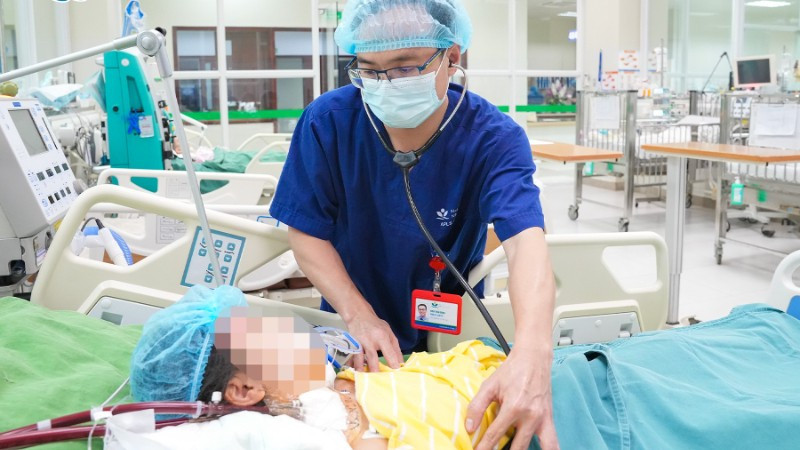
Ba bệnh nhi viêm cơ tim tối cấp được can thiệp ECMO kịp thời trong những ngày nghỉ Tết
Thứ Hai, ngày 23/02/2026 10:33Viêm cơ tim tối cấp ở trẻ em là bệnh lý không hiếm gặp nhưng có thể gây nguy hiểm tính mạng cho trẻ trong thời gian ngắn. Vừa qua, Bệnh viện Nhi Trung ương đã liên tiếp ghi nhận 3...
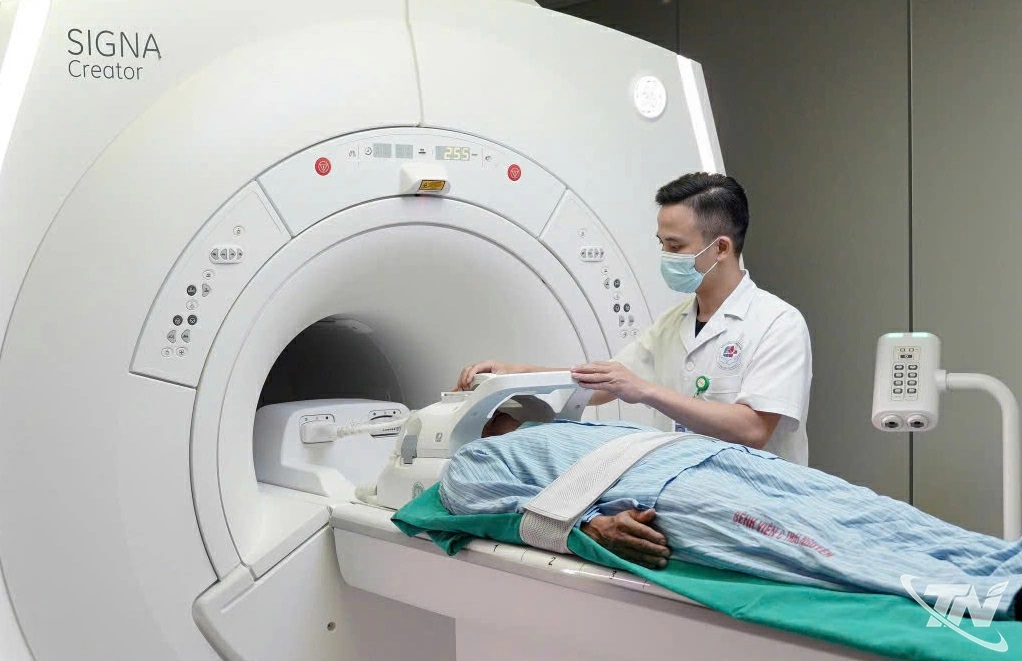
Y tế Thái Nguyên chuyển mình theo hướng hiện đại, thông minh
Thứ Hai, ngày 23/02/2026 10:30Trong tiến trình phát triển nhanh và bền vững, y tế không chỉ là trụ cột bảo đảm an sinh xã hội mà còn là yếu tố quyết định chất lượng nguồn nhân lực và năng lực cạnh tranh của địa phương. Những...
Thông tin các thuốc nhập khẩu sử dụng cho thử nghiệm thuốc trên lâm sàng (MS: DEN-201)
Thứ Năm, ngày 12/02/2026 08:32
Hơn 510.000 lượt người bệnh khám, cấp cứu trong 8 ngày Tết
Thứ Bẩy, ngày 21/02/2026 16:52Bộ Y tế cho biết trong 8 ngày nghỉ Tết Bính Ngọ, các cơ sở y tế đã tiếp nhận thăm khám và cấp cứu hơn 510.000 lượt người bệnh; thực hiện hơn 20.300 ca phẫu thuật; Các bác sĩ cũng chào đón hơn...
Chất lượng dân số: Nền tảng cốt lõi cho khát vọng thịnh vượng và sự trường tồn của dân tộc
Chủ Nhật, ngày 21/02/2026 17:00Chất lượng dân số là sức mạnh nội sinh của mỗi quốc gia. Đối với Việt Nam, khi “con tàu” đất nước đang vươn mình ra biển lớn, vấn đề chất lượng dân số càng trở nên quan trọng, quyết định sự hưng...
Điều kiện mở phòng khám tư nhân
Thứ Bẩy, ngày 21/02/2026 16:56Nội dung câu hỏi: Tôi là bác sĩ y học dự phòng, có chứng chỉ thực hành 12 tháng và đã có giấy phép hành nghề. Xin hỏi, tôimuốn mở phòng khám hoặc cơ sở trị liệu, chăm sóc ban đầu tại nơi cư...
Tạo nền tảng cho y tế hiện đại, vì sức khỏe Nhân dân
Thứ Bẩy, ngày 21/02/2026 16:55Nhìn lại chặng đường một năm đã qua, ngành y tế Thanh Hóa có thêm cơ sở để tự tin khi chuyển đổi số và triển khai Đề án 06 của Chính phủ đã từng bước đi vào chiều sâu, tạo ra những chuyển biến rõ...
Tiếp tục định hình diện mạo y tế số, nâng cao hiệu quả phục vụ người dân
Thứ Bẩy, ngày 21/02/2026 16:50Hơn 34 triệu sổ sức khỏe điện tử đã được tích hợp trên VNeID, 1.210 bệnh viện triển khai bệnh án điện tử. Những bước tiến này đang từng bước định hình diện mạo y tế số và mở ra nhiều lợi ích cho...
Những người giữ mạch sống nơi đầu sóng
Thứ Bẩy, ngày 21/02/2026 16:28Giữa trùng khơi Bạch Long Vĩ, vượt qua thời tiết khắc nghiệt và thiếu thốn, những chiến sĩ áo blouse trắng vẫn lặng lẽ bám đảo, giữ gìn sức khỏe, mạch sống nơi đầu sóng ngọn gió của Tổ quốc. ...
'Cửa ngõ cấp cứu' của Bệnh viện Bạch Mai, bệnh nhân nặng tăng vọt những ngày Tết
Thứ Bẩy, ngày 21/02/2026 16:088 ngày nghỉ Tết Bính Ngọ, các y bác sĩ của Bệnh viện tuyến đầu Bạch Mai đã 'tạm quên Tết' để dành tâm, trí, sức cho người bệnh. Số bệnh nhân nặng đến cấp cứu tại Bệnh viện Bạch Mai tăng mạnh từ...
Nghị quyết và hành động thực chất
Thứ Sáu, ngày 20/02/2026 10:32Mùa Xuân năm nay đến trong bối cảnh đặc biệt khi toàn Đảng, toàn dân, toàn quân đang khẩn trương, quyết liệt đưa Nghị quyết Đại hội XIV của Đảng vào cuộc sống. Không khí ấy khiến mùa Xuân...
Chấn thương mắt nghiêm trọng do pháo nổ dịp Tết Nguyên đán
Thứ Sáu, ngày 20/02/2026 10:28Khoa Mắt, Bệnh viện Bạch Mai đã tiếp nhận liên tiếp nhiều trường hợp chấn thương mắt nghiêm trọng do pháo nổ trong những ngày nghỉ Tết vừa qua. Không ít trường hợp đối mặt nguy cơ...
Chia gan để ghép giúp sự sống được nhân đôi
Thứ Sáu, ngày 20/02/2026 10:26Trong ghép tạng, ghép gan đã khó, thì chia gan để ghép lại càng khó hơn. Thật tự hào khi các thầy thuốc Việt Nam đã chinh phục và làm chủ được kỹ thuật khó đó. Các bác sĩ...
Người bệnh ở lại Tết vẫn chờ từng đơn vị máu, tiểu cầu
Thứ Sáu, ngày 20/02/2026 10:18“Tết lúc nào cũng có nhưng cơ hội chữa bệnh cho con chỉ có một”, đó là tâm sự của một người mẹ có con đang điều trị ung thư máu phải ở lại bệnh viện những ngày Tết. Sau một năm ngược...
Tết không nghỉ trong phòng chạy thận
Thứ Sáu, ngày 20/02/2026 10:16Giữa không khí Tết rộn ràng, nhưng trong phòng chạy thận vẫn duy trì nhịp điều trị quen thuộc. Nhiều bệnh nhân phụ thuộc vào máy móc và khung giờ cố định, không thể gián đoạn dù chỉ một buổi. ...
Những người bám trụ nơi biên viễn
Thứ Sáu, ngày 20/02/2026 10:14Giữa những vùng núi xa xôi, nơi điều kiện kinh tế - xã hội còn nhiều khó khăn, y tế cơ sở rất quan trọng đối với sức khỏe người dân. Ở đó, mỗi người thầy thuốc không chỉ đảm nhận vai trò khám...
Nâng cao chất lượng thụ hưởng bảo hiểm y tế
Thứ Sáu, ngày 20/02/2026 10:12Thực hiện Nghị quyết Đại hội đại biểu toàn quốc lần thứ XIII của Đảng, cùng với mục tiêu phát triển kinh tế-xã hội nhanh và bền vững, việc bảo đảm an sinh xã hội tiếp tục được xác định là một trụ...

.jpg)
.jpg)
.jpg)